分子轨道(Molecular Orbital)理论是现代共价键理论之一,区别于杂化轨道理论研究原子中电子的杂化,分子轨道理论主要研究分子中原子的杂化(成键)。在杂化轨道理论中,化学家假想每一个原子或者说每一根键都是孤立的(定域的),这造成了很多问题,例如苯分子或共轭二烯的离域键,都无法直接解释,Pauling引入的“共振”概念其实是针对这些不足的打补丁;但这些现象在分子轨道理论中的解释却可以天然地全面。到如今,杂化轨道理论经过不断完善,也是成熟的共价键理论了,甚至也可以被用于理论计算;但在普通化学中,我们介绍的杂化轨道理论层次很浅,因此使用分子轨道理论解释共价键是一个很好的方法。
虽然本文主要讲解分子轨道理论在有机化学上的应用,但我认为还是应该先温习一下分子轨道理论(指在无机或者说结构层面)。氢原子成H-H键时分子轨道:
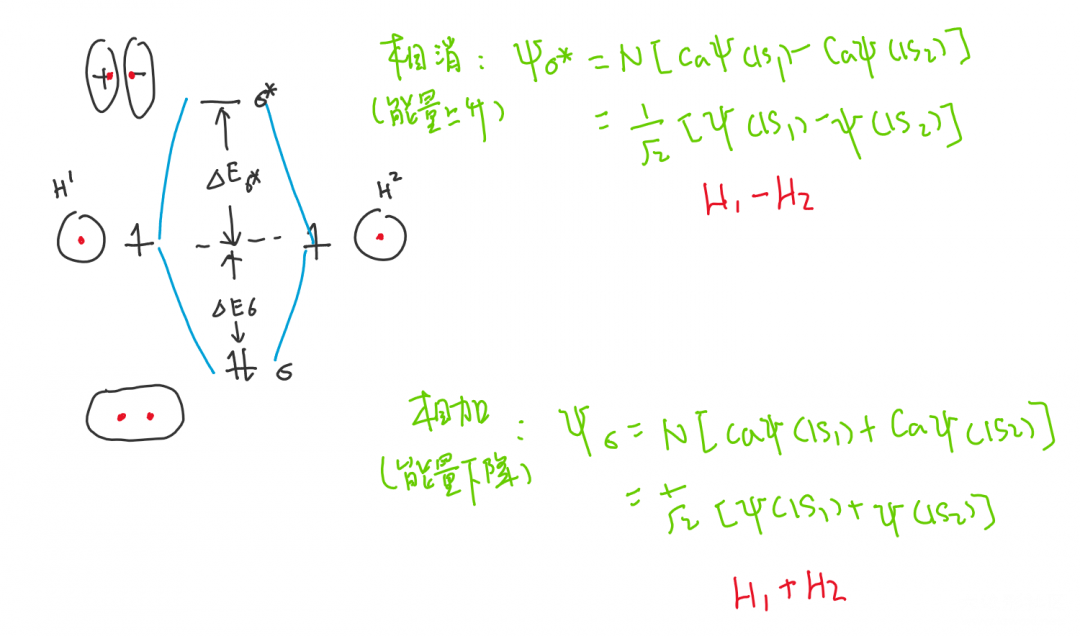
两个氢原子的轨道相加或相减,分别形成了一个σ成键轨道和一个σ*反键轨道。成键轨道中电子集中分布于原子核之间,能量很低;而在反键轨道中(图中正负表示相位相反,亦可颠倒顺序;概率密度为|ψ|²,因此电子密度相同),电子集中分布于原子核两侧,在原子核中间的位置,没有电子分布,形成波节node.分子轨道理论中常常通过波节比较分子轨道的稳定性,原子核之间的位置是成键效果最好的位置,最稳定,但有了波节这个好位置就不能填充电子了,因此波节越多说明轨道能量越高,不稳定;进一步讨论,每次原子轨道的相加都意味着一次能量的降低,而相消意味着一次能量的升高。
原子间杂化时(杂化轨道是电子的杂化,分子轨道是原子的杂化,我这边说杂化应该也没啥问题),轨道也遵守能量或数量的守恒,因此在本例子中,σ和σ*与原轨道的能量差值△E互为相反数。(对待复杂分子,轨道相加和相消时降低或上升的能量也近似相等,在粗糙的有机化学上常常使用这一特点,用直接“计算”的方法解释稳定性或者判断选择性。)H-H杂化时有两个电子,杂化后都填入了最低能量的σ成键轨道,能量成功降低。
在国内外89.3%(要素)的教材都是通过氧分子的顺磁性引入分子轨道理论的。氧原子的2s电子占满了成键与反键轨道,相抵消,即没有成键,没有什么意义;我这里只画了两个氧原子2p轨道的杂化情况:
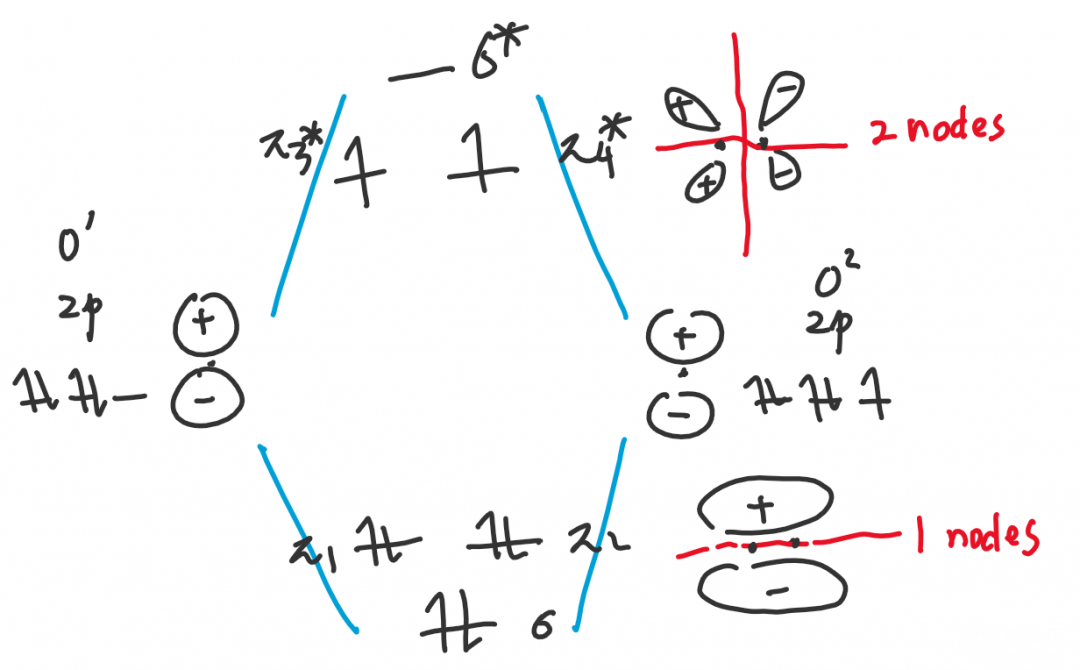
根据上面有关H-H杂化的详细解释,大家不难理解氧原子2p轨道的成键。在无机中,很少有老师在讲到此处时不会像话痨一样讲,很明显在图上,π₃ π₄都有单电子,因此氧气顺磁性,这是杂化轨道理论所不能解释的...blablabla...。但在有机中,我们会提到另一个内容:氧气的单线态¹O₂与三线态³O₂。上图常见的是三线态氧(基态),余下的两个电子成单排列;通过光敏剂的激发,氧气会形成单线态(激发态),余下的两个电子也成自旋相反的电子对。
在有机化学中,非自由基反应通常涉及的都是电子对的迁移,因此当想要通过氧气将过氧链加入有机分子时(氧气的电子对加成到双键上),一定需要通过单线态氧,而三线态氧就做不到了。激发的过程通常随反应一同进行,例如在氧气做“二烯”的D-A反应中,用玫瑰红光敏剂(Rose Bengal)和光照即可顺利进行反应。
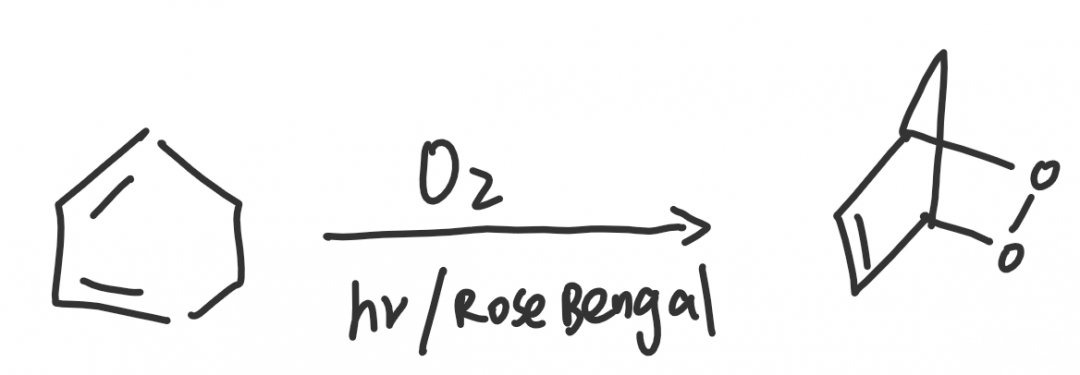
今天有些累,先更新分子轨道对共轭二烯稳定性的解释,有时间再更新周环反应里分子轨道理论对立体选择性的解释。我们直接通过乙烯和1,3-丁二烯的分子轨道,来说明一下有机里面粗糙而更实用的分子轨道表示方法和规定。如下:
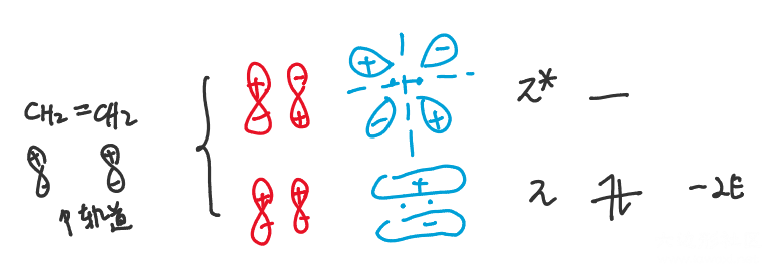
学习有机时,一个常见的思路就是要关注具体的位置,不能像无机一样妄想集大成。例如我们在研究普通烯烃和共轭二烯的稳定性,关注的应当是双键中的第二根键,也就是四个π轨道,那么我们索性不把σ轨道画出来。在之前的O=O键中,我们展示了p轨道分别相加或相消的情况,如蓝色表示;图示方法固然值观,但对于复杂分子很难画,因此我们简化成了左侧的红色,即想象中的“杂化前一瞬间的排列方式”。因此判断波节的个数,也就可以直接画一条直线,分割两个区域,看两个区域的相位(正负)是否正好相反即可了,大家自行体会。
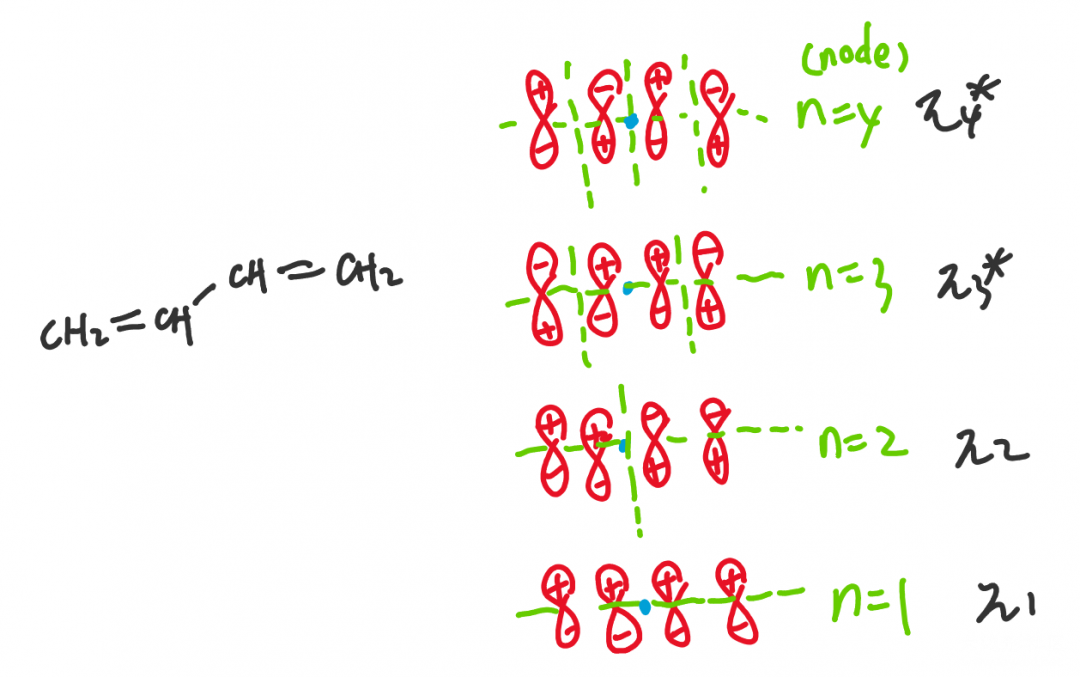
这张图展示的是1,3-丁二烯的分子轨道图示,其中绿色虚线是标出的波节。(大家会发现波节是交替排列的)如果说π₁和π₄*大家好理解的话,中间的两个轨道就显得很难理解了:“虽然我通过计算知道你这种排法确实是从上至下越来越稳定的,但画之前你是怎么排出来的呢?”这涉及分子轨道的规律:①中心对称性依次变化(我用蓝色笔表示出了中心,两侧相位的变化依次是中心对称u,反中心对称g,中心对称...的循环);②波节数按自然数依次上升。
之前我们说过,对于能量高低,我们可以粗略地按相消一次+E,相加一次-E来计算。(非常粗糙,只是数量级相近,帮助我们计算稳定性大小而已)那么普通烯烃两个电子都下降E,如果是孤立二烯烃,则杂化后能量降低4E;共轭二烯烃中,两个电子下降2E,两个电子下降E,因此共轭二烯烃杂化后能量下降6E,显然比普通烯烃更稳定。
解释完了。😀
