对于一个电化学装置,我们可以通过热力学计算(法拉第定律...)的方法得到电动势(E),同样可以通过实际测量电池两端输出或输入电压获得路端电压(U)。在原电池中,路端电压往往会比电动势小;在电解池中,路端电压往往大于电动势;这些额外的能量转换成了热量而散失。这两者有区别的原因在于,电池电压的影响因素不仅仅是热力学的电势差/转移电子数,还包含一些其他的动力学因素甚至物理因素,我们笼统地用“超电势Overpotential(η)”来讨论。
In electrochemistry, overpotential is the potential difference (voltage) between a half-reaction's thermodynamically determined reduction potential and the potential at which the redox event is experimentally observed.
—— Wikipedia: Overpotential
1.氢气在汞阴极表面析出有动力学阻碍,而铂甚至铁都容易析氢。利用这一特点,用汞电解氯化钠溶液可以制得钠单质。(由于钠和水反应析氢,有动力学阻碍;又因为钠与汞结合形成合金,及时隔离开水体系)
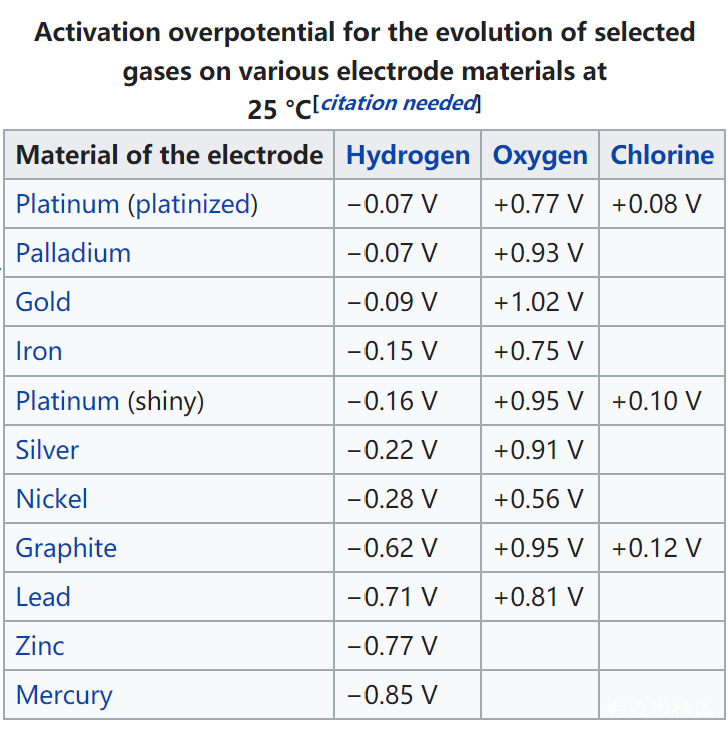
2.电解氯化钠水溶液时,氯离子被氧化为氯气,而不是水分子被氧化为氧气。实际上,前者的半反应EΘ=1.36V,后者半反应EΘ=1.23V。根据热力学理论,相同浓度下应该是水更容易被氧化,况且是在氧多的情况下。实验中的反常表现,是由于电极表面有Bubble overpotential,使失电子形成气体很不顺畅,由于氯离子氧化和水分子氧化所失去的电子比例为1:2,因此氯气析出相较于氧气显得稍微容易。
在没有电流通过时,电化学装置处于平衡状态,内部反应可逆,此时两端电极电势称为平衡电极电势;当有电流通过时,电极电势偏移平衡电极电势,这种现象称为“电极极化”。超电势的概念就是定义在电极极化上的。超电势产生条件大概分为以下几种(维基百科上摘录的,我个人认为好像没什么用?):
- 电解池的阳极更正,消耗的能量超过热力学所需的能量。
- 电解池的阴极更负,消耗的能量超过热力学所需的能量。
- 原电池的阳极不那么负,释放的能量比热力学上的少。
- 原电池的阴极不那么正,比热力学上提供的能量更少。
当然,按照以上概念,当电流密度( current density,单位A/m2)增大时,偏离可逆状态越远,电极极化加深,超电势大。因此可以将超电势随电流密度增大而增大的规律总结为经验公式(电催化析氢研究很透彻,这两个公式都是专门计算析氢的,其他反应暂不了解是否有方程):Bulter-Volmer方程,和其改进版Tafel方程。A为常数Tafel slope.
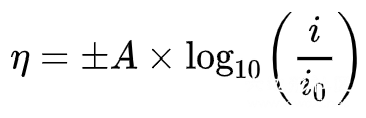
Tafel方程相比于Bulter-Volmer方程稍显精准,但作为经验公式,它们的计算结果和实际测量还是相差较远。这是由于在电化学装置反应过程中,每一个步骤都会引发多种形式的超电势,我们所总结的η是这些超电势的总和。不仅仅受电流密度影响,对于一个相同的反应,甚至是操作条件都会对超电势有影响。超电势的分类如下。
(超电势的本质是电极极化,这些分类的英文名称是XX Overpotential,但中文是XX极化,不要怀疑)
1.浓差极化 Concentration overpotential
溶液中各处的浓度有差别,扩散缓慢,导致了很多电能以热量散失,这就是浓差极化。可能造成的原因有,电子导体中电子浓度较高,与离子浓度不适配;电化学装置运行一段时间后,携带电荷的两种离子浓度减小,尤其是当它们比溶液本体浓度更小时,超电势十分明显。前文氯气和氧气谁先析出,由于Bubble overpotential,是浓差极化的一个细分。气体分子在溢出时会在电极表面形成气泡(Bubble),使电极与溶液接触面积减小,导致了局部电流密度增大,使得超电势增大。

2.电化学极化 Reaction overpotential(或称活化超电势 Activation overpotential)
电化学超电势是由反应的活化能引起的超电势现象,我们考虑△G,只考虑了反应的热力学有利,而没有考虑动力学上是否可以反应。当考虑到活化能时,这也是为什么氢气容易在有催化效果的铂电极上析出,而对于没有这种能力的锌、汞电极都不能有效地析出(称之为动力学阻碍)。在电化学反应中,为什么选用铂电极,一是为了它的电化学惰性,二是贪图它对超电势的削弱,这是热力学和动力学共同的决定。
3.有争议的:电阻超电势 Resistance overpotential
这种超电势不是由于电极极化引起的,而是由于电路或电池的设计和物理属性产生的。例如电池内阻,电极与溶液间的junction overpotential,离子吸附在电级上形成bilayer(是电容)。在Wikipedia上,这一项列入超电势;而在国内教材或文献中,这一项单列出来,属于影响电动势与路端电压的另一因素。
1.Wikipedia: https://en.wikipedia.org/wiki/Overpotential
2.Wikipedia: https://en.wikipedia.org/wiki/Tafel_equation
3.雷越,黄春华,冯振华,荆延,陈飞武,王桂华.电极表面超电势Tafel公式的推广[J].大学化学,2013,28(06):62-65.
4.尤蕾蕾,潘志刚.有关电解的概念及原理[J].化学教学,2010(10):1-5.
